The significance of DOPEY2 expression in TMPRSS2-ERG gene fusion-negative prostate cancer
Luo Zihuan, Lu Minhua, Huang Qunxiong, Zhang Lingxiao, Chen Xiaobo, Gao Xin, Li Liaoyuan.
Department of Urology, the Third Affiliated Hospital of Sun Yat-sen University, Guangzhou 510630, China
Keywords: Prostate cancer ; TMPRSS2-ERG ; ERG ; DOPEY2 前列腺癌是欧美国家男性最常见的恶性肿瘤,发病率居首位,致死率仅次于肺癌 [1] 。在我国,随着人口老龄化、饮食结构改变和医疗诊断技术的提高,前列腺癌的发病率逐年升高 [2-3] 。针对前列腺癌发生发展的相关研究成为世界范围内的热点。 Tomlins等[4-5] 2005年在 Science杂志上首次报道前列腺癌中存在 TMPRSS2-ERG 融合基因改变现象,在
DOI : 10.3877/cma.j.issn.1674-3253.2016.02.015
目的 探讨 DOPEY2在 TMPRSS2-ERG基因融合阴性前列腺癌中的表达及其临床意义。方法 本研究通过 RT-PCR和 Western Blot技术检测前列腺癌细胞株 VCaP和 PC-3中 ERG和 DOPEY2的表达情况,同时,采用免疫组化技术检测 46例前列腺癌根治术后的石蜡标本中 ERG和 DOPEY2的表达情况,分析两者的表达以及与临床病理特征之间的关系。结果 DOPEY2在 TMPRSS2-ERG基因融合阳性前列腺癌细胞株 VCaP中的 mRNA和蛋白表达水平,均比 TMPRSS2ERG基因融合阴性前列腺癌细胞株 PC-3低,且差异均有统计学意义( P<0.05)。免疫组化结果显示, DOPEY2在 TMPRSS2-ERG基因融合阴性组织中的阳性表达率高于基因融合阳性组( 76.5%和
Objective To study the difference and clinical significance of DOPEY2 expression between TMPRSS2-ERG gene fusion-positive and TMPRSS2-ERG gene fusion-negative prostate cancer. Methods The expressions of ERG and DOPEY2 in two prostate cancer cell lines (VCaP and PC-3) were examined by RT-PCR and Western Blot. Then, immunohistochemistry was used to detect the expression of ERG and DOPEY2 in 46 cases of prostate cancer. Results The mRNA and protein expression levels of DOPEY2 in TMPRSS2-ERG gene fusion-negative cell line (PC-3) were significantly higher than that in TMPRSS2-ERG gene fusion-positive cell line (VCaP, P<0.05). The results of immunohistochemistry showed that the expression ratio of DOPEY2 in ERG-negative and ERG-positive prostate cancer was 76.5% and 33.3% respectively (P<0.05). In addition, DOPEY2 was positive correlated with Gleason Grade and T stage (P<0.05). Over-expression ratio of ERG protein was 26.1% (12/46), and it had significant correlation with low Gleason score (P<0.05), while not with age, serum PSA levels, T stage and metastasis. Conclusion s There is a significant inverse correlation between the expression of ERG and DOPEY2 in both prostate cell lines and cancer tissues. DOPEY2 can serve as a helpful and prognostic biomarker in prostatic cancer.
引言 前列腺癌是欧美国家男性最常见的恶性肿瘤,发病率居首位,致死率仅次于肺癌 [1] 。在我国,随着人口老龄化、饮食结构改变和医疗诊断技术的提高,前列腺癌的发病率逐年升高 [2-3] 。针对前列腺癌发生发展的相关研究成为世界范围内的热点。 Tomlins等[4-5] 2005年在 Science杂志上首次报道前列腺癌中存在 TMPRSS2-ERG融合基因改变现象,在西方国家前列腺癌人群中的发生率约为 50% ~70%,具有前列腺癌特异性且在肿瘤发生早期就有出现,但融合基因的发生与前列腺癌临床预后之间关系尚存在争议。DOPEY2是人类 DOPEY家族成员之一,具有亮氨酸拉链结构域,在蛋白交互作用中发挥重要作用,早期研究提示该蛋白与唐氏综合征的发病相关 [6] 。而 DOPEY2在人类肿瘤疾病,尤其是前列腺癌的发生发展中有无扮演重要角色,尚无文献报道。因此,本实验通过 RT-PCR、 Western Blot和免疫组化技术,分别检测前列腺癌细胞株和人体前列腺癌组织标本中 ERG和 DOPEY2的表达情况,初步探讨二者在前列腺癌生物学进展中的相互关系及临床意义。
1 资料与方法
1.1 细胞与标本
TMPRSS2-ERG基因融合阴性前列腺癌细胞株 PC-3和 TMPRSS2-ERG基因融合阳性前列腺癌细胞株 VCaP均购自美国 ATCC细胞库,由科室实验室于液氮中长期保存。细胞培养: PC-3和 VCaP分别采用 Gibco公司 RPMI 1640培养基和 DMEM高糖培养基,配以 10%胎牛血清,于 37℃、5%CO2培养箱中培养。2~3 d更换培养液,以 0.25%的含 EDTA胰蛋白酶消化贴壁细胞并传代,取对数生长期的细胞用于实验。
选取中山大学附属第三医院泌尿外科,自 2006年 1月至 20012年 12月份期间的 46例前列腺癌根治术后组织标本。记录患者的手术年龄、术前 PSA值、 Gleason评分、T分期和有无远处转移等临床病理特征数据。
1.2 RT-PCR检测细胞中 ERG和 DOPEY2 mRNA的表达
RNA的提取与逆转录:取 25 cm2 规格培养瓶,待贴壁细胞融合约 90%时,每瓶加入 Trizol 2 ml,严格按照 Trtizol法步骤提取总细胞 RNA,并测量浓度。取细胞总 RNA1 μg,反应体系 20 μl,参照 TaKaRa逆转录试剂盒造作说明,合成 cDNA后,于-20 ℃保存备用。
目的基因在细胞系中的表达:目的基因 ERG和 DOPEY2以及内参基因 GAPDH的引物由广州行知生物有限公司合成提供。ERG的上下游引物分别为: ERG-F5’-TTATCGTGCCAGTAGCAGGT-3’,ERG-R 5’-GATGTTGACGTCTGGAAGGC-3’;DOPEY2的上下游引物分别为: DOPEY2-F 5’-CCTTTTCGCGTCCTCATCAG-3’,DOPEY2-R 5’-AAAGGCCCTGATGACTTCGA-3’;GAPDH的上下游引物分别为: GAPDH-F 5’-ACAACAGCCTCA AGATCA TCAG-3’,GAPDH-R 5’-GGTCCACCACTGACA CGTTG-3’;采用 SYBR誖Green I* 嵌合荧光法进行实时定量 PCR,反应体系 20 μl,严格按照 TaKaRa公司试剂盒的操作说明上样,每个标本做 3个复孔,每次反应各个引物各设一个阴性对照。使用 ABI 7500附带的分析软件分析结果,以内参 GAPDH dCt的均值为对照,观察各细胞系中的基因表达情况。
1.3 Western Blot检测细胞中 ERG和 DOPEY2蛋白的表达
向每瓶细胞培养瓶中加入 400 μl混合好的蛋白裂解液,严格按照凯基公司生产的全蛋白提取试剂盒的操作步骤进行。将提取好的蛋白,通过 BCA法测定蛋白浓度,于-80 ℃保存备用。按照说明书配制 10%分离胶和 5%浓缩胶,取 40 μg蛋白的上样量与上样缓冲液 Loading Buffer预混好,并加热使得蛋白变性。上样后,浓缩胶以 80 V恒压电泳约 30 min,再以 120 V恒压电泳约 90~120 min。转膜条件, 200 mA恒流 2h。成功转膜后将 PVDF膜室温下封闭( 5% BSA溶液) 1h,一抗杂交孵育 4 ℃轻摇过夜( ERG 1:1000,Abcam;DOPEY2 1:300,Abcam; GAPDH 1:1000,Abcam)。回收一抗, TBST洗膜三次后,根据一抗种属来源不同加入 1:2000 HRP标记的羊抗兔或羊抗鼠二抗,室温孵育 1.5 h,再次洗膜,于暗室采用 ECL法显色曝光,目的条带采用 Image J软件进行灰度分析。
1.4 免疫组化技术检测组织标本中 ERG和 DOPEY2蛋白的表达
采用免疫组化 SP法,所有操作步骤均严格按照北京中杉金桥生物技术有限公司免疫组化试剂盒说明书进行。将石蜡包埋的前列腺癌组织以 4 μm连续切片,晾干后置于烤箱中 60 ℃烤片 1h。常规脱蜡水化;使用 3% H2O2,微波炉低火档 5 min,以去除内源性过氧化物酶,再利用 10 mmol柠檬酸钠 ,高温高压进行抗原修复,冷却至室温,去离子水和 PBS各漂洗2 次,5min/ 次;一抗孵育4 ℃过夜,对同一蜡块的2 张切片,分别滴加50 μl DOPEY2 (1:100)和ERG (1:100);次日,PBS 冲洗3 次,5min/ 次,甩干,滴加二抗,37 ℃恒温箱中孵育15 min,PBS 冲洗3 次,5 min/ 次,甩去冲洗液,DAB 显色,苏木素复染、清水冲洗、脱水、透明、封片。免疫组化结果评分,通过对组织切片中阳性细胞百分比及着色的深浅来对染色结果进行半定量分析。阳性染色细胞百分率定义如下,0 分:阴性,1 分:≤10%,2 分:11%~50%,3 分:51%~75%,4 分:>75%;染色强度评分标准如下:0 分:无着色或与背景均匀一致的淡黄色,1分:浅黄色,2 分:棕黄色,3 分:棕褐色。前后两项相乘:0~3 分为(-),3 分为(+),4 分为(++),5 分以上为(+++)。
1.5 统计学分析
数据结果采用MedCalc 11.4.2.0 统计软件进行分析,计量资料比较采用t 检验,定性资料比较采用χ2 检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 不同前列腺癌细胞株中 ERG和 DOPEY2的 mRNA表达水平
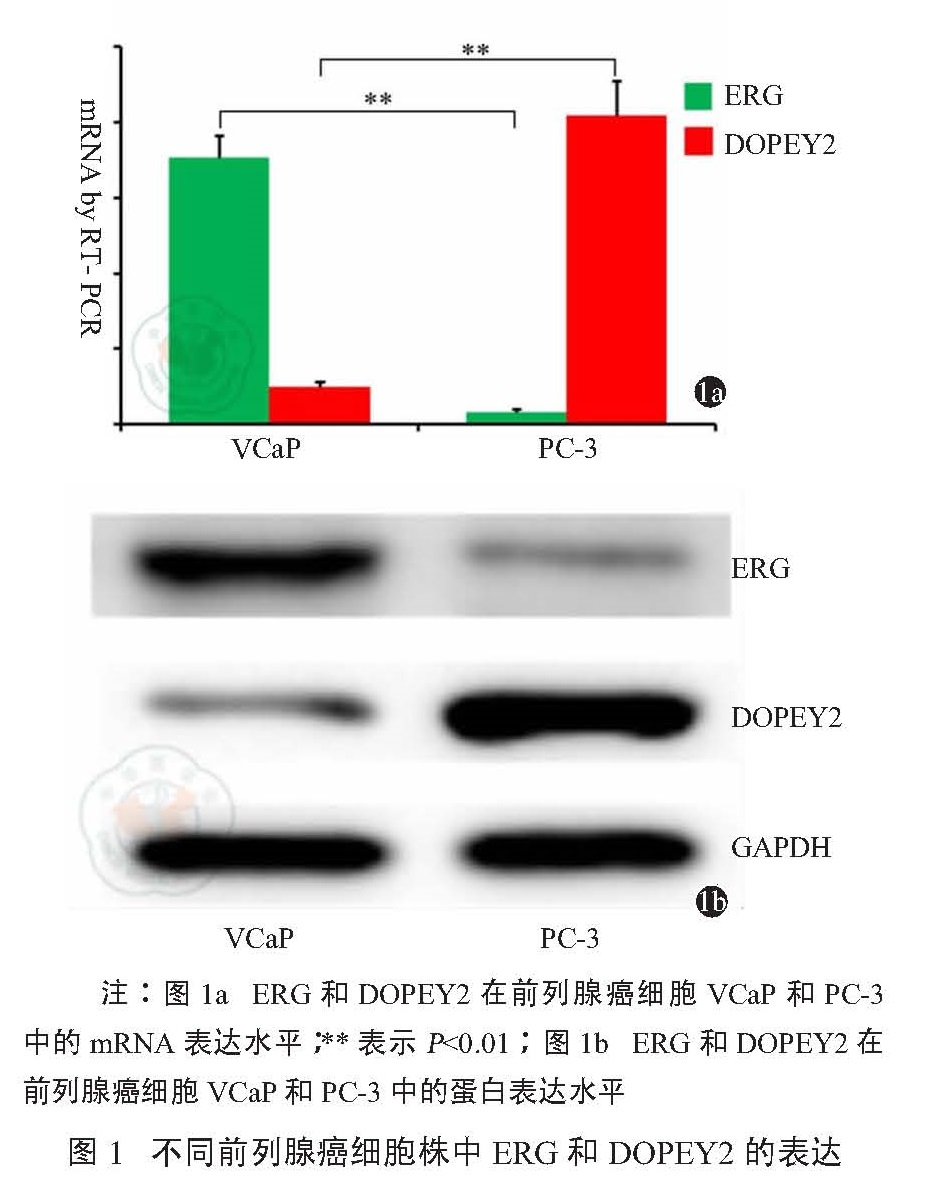
通过提取前列腺癌细胞株 VCaP和 PC-3中总 RNA,以逆转录合成的 cDNA为转录模板进行实时定量 PCR,扩增目的基因,分别比较 VCaP和 PC-3细胞株中, ERG和 DOPEY2的表达水平差异。实验结果表明, ERG在 TMPRSS2-ERG基因融合阳性的前列腺癌细胞株 VCaP中表达明显高于基因融合阴性的细胞株 PC-3,相对变化倍数分别为: [(7.06± 0.6)和( 0.32±0.09),P<0.01];然而,相比较于 VCaP, DOPEY2在 TMPRSS2-ERG基因融合阴性的前列腺癌细胞株 PC-3中的表达要高,相对变化倍数分别为: [(1.08±0.15)和( 8.19±0.9),P<0.01]。结果见图1 a。
2.2 不同前列腺癌细胞株中 ERG和 DOPEY2的蛋白表达水平
利用 Western Blot技术检测前列腺癌细胞株 VCaP和 PC-3中 ERG和 DOPEY2的表达情况,蛋白条带进一步采用灰度分析软件 Image J进行定量差异分析。结果显示, ERG在 VCaP中蛋白表达水平明显高于基因融合阴性的细胞株 PC-3,相对灰度分析值为:([ 1.12±0.04)和( 0.42±0.03),P<0.05];而比较 DOPEY2在 VCaP和 PC-3中的蛋白表达水平,前者明显低于后者,相对灰度分析值为:([ 1.39±0.05)和(0.33±0.04),P<0.05]。结果见图1 b。
注:图 1a ERG和 DOPEY2在前列腺癌细胞 VCaP和 PC-3中的 mRNA表达水平; **表示 P<0.01;图 1b ERG和 DOPEY2在前列腺癌细胞 VCaP和 PC-3中的蛋白表达水平
图1 不同前列腺癌细胞株中 ERG和 DOPEY2的表达
2.3 免疫组化检测 ERG和 DOPEY2在前列腺癌组织中表达
人前列腺癌组织中, ERG蛋白阳性染色呈淡黄色至棕黄色颗粒状,定位于细胞核,细胞膜和细胞质着色视为非特异性染色; DOPEY2蛋白阳性染色呈淡黄色至棕黄色,定位于细胞质和细胞核。纳入检测的 46例前列腺癌标本中, ERG和 DOPEY2的阳性表达率分别为 26.1%(12/46)和 65.2%(30/46)。有趣的是在 ERG阳性表达的前列腺癌标本中 DOPEY2的阳性率为 33.3%(4/12),而在 ERG阴性表达的前列腺癌标本中 DOPEY2的阳性率可达 76.5%(26/34)。免疫组化结果见图 2。
2.4 ERG和 DOPEY2与前列腺癌临床病理特征的关系
ERG的表达与前列腺癌的 Gleason分级的相关性具有统计学意义( P<0.05),ERG阳性的患者具有较低的分级。而患者的年龄、血浆 PSA值,病理 T分期和远处转移等参数与 ERG的表达均无相关。另一方面, DOPEY2的表达与肿瘤的 Gleason分级和病理 T分期存在一定正相关( P<0.05),随着肿瘤分级和病理分期的升高, DOPEY2的表达增强。其余病理指标与 DOPEY2的相关性差异无统计学意
注:a、b和 c分别对应 ERG蛋白的 -/+、++和 +++三个免疫组化评分判定结果, d、e和 f分别应对同一组织块的 a、b和 c,免疫组化评分判定结果分别为:+++、++和 -/+
图2 ERG和 DOPEY2在前列腺癌组织中的表达情况
义(表 1)。
3 讨论 Tomlins等[4] 在 Science杂志上首次在前列腺癌中发现 TMPRSS2基因可以通过染色体内或染色体间的重排和 ETS家族基因融合(其中以 ERG最为常见,占比达 90%),从而诱导了依赖于雄激素效应基因的表达增强。2010年 Scheble等[7] 利用近 50多种不同组织来源肿瘤标本,应用 FISH法检测 TMPRSS2-ERG基因融合,发现除前列腺癌外,均未发现 TMPRSS2-ERG基因融合,由此表明 TMPRSS2ERG基因融合是前列腺癌的特异性基因改变。由于90.9%存在 TMPRSS2-ERG融合基因的前列腺癌中发现 ERG过表达,有研究通过采用免疫组化技术发现 ERG蛋白的表达和 ERG基因的重排之间存在显著地一致性,因此,可通过检测 ERG的表达作为 TMPRSS2-ERG基因融合的高特异性和敏感性的标志物 [8] 。当前针对 TMPRSS2-ERG融合基因的研究主要集中在前列腺癌的诊断和预后检测方面。课题组前期研究发现基因融合可用于前列腺癌的早期诊断,其敏感性和特异性均在 80%以上 [9] ,进一步通过 FISH技术发现 TMPRSS2-ERG基因畸变率大于 2.6%时,其诊断前列腺癌淋巴转移的敏感性为80.4%,特异性为 85.1%,提示 TMPRSS2-ERG基因融合可能是前列腺早期转移的一个关键分子事件 [10] 。另外,通过对前列腺增生,低、高级别上皮内瘤变以及前列腺癌的穿刺标本,联合检测 PCA3和 TMPRSS2ERG,可以有效区分出肿瘤,诊断率可达 90%[11] 。 Sanguedolce等[12] 进一步在尿液标本中检测 PCA3和 TMPRSS2-ERG,通过联合血清 PSA结果诊断前列腺癌,特异性为 90%,敏感性为 80%,同时指出, TMPRSS2-ERG不仅在有助于前列腺癌的诊断,
表1 ERG 和DOPEY2 蛋白在前列腺癌中的表达及其与临床病理特征的关系
还能有效区分进展性和惰性前列腺癌。
DOPEY2是人类 DOPEY家族成员之一,早期研究提示该蛋白与唐氏综合征的发病相关。通过对唐氏综合征患者临床、细胞遗传和分子发生等数据分析,鉴定出唐氏综合症染色体区 -1(down syndrome chromosomalregion-1,DCR-1),而 DOPEY2作为 DCR-1区域新发现的转录因子,被认为在唐氏综合症患者大脑胚胎发育,神经改变以及智力迟滞发育方面扮演了重要角色 [13] 。DOPEY家族蛋白具有亮氨酸拉链结构域,在蛋白交互作用中发挥重要作用,参与胚胎发生,细胞分化以及细胞周期调控等生物学进程 [14] 。为探究 DOPEY2在人类前列腺癌的发生发展中的作用,本研究首先通过细胞水平,利用 RT-PCR和 Western Blot技术发现 DOPEY2不论是基因转录水平还是蛋白翻译水平,在不同的 TMPRSS2-ERG基因融合状态间的表达存在差异。随后,我们利用免疫组化技术检测前列腺癌组织标本中的 ERG和 DOPEY2的表达情况,发现二者在前列腺癌中的表达呈负相关, ERG阴性标本中的 DOPEY2阳性率高于 ERG阳性标本。提示 TMPRSS2-ERG基因融合有可能负调控 DOPEY2的表达,进一步影响肿瘤的发生发展。研究进一步分析了 ERG和 DOPEY2分别与前列腺癌患者年龄、血浆 PSA值, Gleason分级,肿瘤病理分期和远处有无转移等临床指标的关系。TMPRSS2-ERG基因融合的发生率在低 Gleason评分组较高,而与其他临床病理参数的相关性却不明显,该结果与 Bismar等[15] 研究报道一致。DOPEY2的阳性表达与患者的 Gleason评分以及病理 T分期呈现一定正相关,在高 Gleason评分组和高分期病例中 DOPEY2的阳性率较高,提示 DOPEY2有可能作为一个有用的指导前列腺癌分期及判断预后的分子标记物,但需要进一步的研究阐明其与 ERG的相互作用,以及其潜在的肿瘤分子生物学机制。
图1 不同前列腺癌细胞株中 ERG和 DOPEY2的表达 图2 ERG和 DOPEY2在前列腺癌组织中的表达情况 表1 ERG 和DOPEY2 蛋白在前列腺癌中的表达及其与临床病理特征的关系
[1] Siegel RL, Miller KD, Jemal A. Cancer statistics, 2016 [J]. CA Cancer J Clin, 2016, 66(1): 7-30.
[2] Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015 [J]. CA Cancer J Clin, 2016, 66(2):115-132.
[3] Zhang L, Wu S, Guo LR, et al. Diagnostic strategies and the incidence of prostate cancer: reasons for the low reported incidence of prostate cancer in China [J]. Asian J Androl, 2009, 11(1): 9-13.
[4] Tomlins SA, Rhodes DR, Perner S, et al. Recurrent fusion of TMPRSS2 and ETS transcription factor genes in prostate cancer [J]. Science, 2005, 310(5748): 644-648.
[5] Clark JP, Cooper CS. ETS gene fusions in prostate cancer [J]. Nat Rev Urol, 2009, 6(8): 429-439.
[6] Rachidi M, Delezoide AL, Delabar JM, et al. A quantitative assessment of gene expression (QAGE) reveals differential overexpression of Dopey2, a candidate gene for mental retardation, in Down syndrome brain regions [J]. Int J Dev Neurosci, 2009, 27(4): 393-398.
[7] Scheble VJ, Braun M, Beroukhim R, et al. ERG rearrangement is specific to prostate cancer and does not occur in any other common tumor [J]. Mod Pathol, 2010, 23(8): 1061-1067.
[8] Park K, Tomlins SA, Mudaliar KM, et al. Antibody-based detection of ERG rearrangement-positive prostate cancer [J].Neoplasia, 2010, 12(7): 590-598.
[9] Sun QP, Li LY, Chen Z, et al. Detection of TMPRSS2-ETS fusions by a multiprobe fluorescence in situ hybridization assay for the early diagnosis of prostate cancer: a pilot study [J]. J Mol Diagn, 2010, 12(5): 718-724.
[10] Gao X, Li LY, Zhou FJ, et al. ERG rearrangement for predicting subsequent cancer diagnosis in high-grade prostatic intraepithelial neoplasia and lymph node metastasis [J]. Clin Cancer Res, 2012,18(15): 4163-4172.
[11] Mikhaylenko DS, Perepechin DV, Grigoryeva MV, et al. PCA3 and TMPRSS2: ERG genes expression in biopsies of benign prostate hyperplasia, intraepithelial neoplasia, and prostate cancer [J].Urologiia, 2015, (5): 46-50.
[12] Sanguedolce F, Cormio A, Brunelli M, et al. Urine TMPRSS2: ERG fusion transcript as a biomarker for prostate cancer: literature review [J]. Clin Genitourin Cancer, 2016,14(2): 117-121.
[13] Rachidi M, Lopes C, Costantine M, et al. C21orf5, a new member of Dopey family involved in morphogenesis, could participate in neurological alterations and mental retardation in Down syndrome [J]. DNA Res, 2005, 12(3): 203-210.
[14] Bjorklund M, Taipale M, Varjosalo M, et al. Identification of pathways regulating cell size and cell-cycle progression by RNAi [J]. Nature, 2006, 439(779): 1009-1013.
[15] Bismar TA, Dolph M, Teng LH, et al. ERG protein expression reflects hormonal treatment response and is associated with Gleason score and prostate cancer specific mortality [J]. Eur J Cancer, 2012, 48(4): 538-546.